Rohelise keemia eesmärk on keemiliste mõjutuste vähendamine inimese tervisele ja praktiliselt kõrvaldada keskkonnasaastamine spetsiaalsete, jätkusuutlike ennetusprogrammide kaudu. Roheline keemia otsib alternatiivseid, keskkonnasõbralikke reaktiive ning püüdleb samal ajal reaktsioonide kiiruse suurendamise ja madalamate reatksioonide temperatuuride poole.
Rohelise keemia kontseptsioon rakendab uuenduslikke teaduslikke lahendusi laboris püstitatud keskonnaprobleemide lahendamiseks. Orgaaniline keemik Paul T. Anastan, kes töötab Keskkonnakaitseagentuuri (EPA) Saastekontrolli ja Mürgistuste Osakonnas, ja John C. Warner töötasid 1991. aastal välja „Rohelise keemia kaksteist põhimõtet“. Need põhimõtted võib grupeerida kaheks – riskide vähendamine ja ökoloogilise jalajälje minimeerimine.
Riskide vähendamine laboratooriumis
Sigma-Aldrich on pühendunud alternatiivsete toodete loomisele, pidades silmas oma töötajate, klientide ja rahva tervist ja ohutust.
- Kasutage turvalisemaid kemikaale – Kasutage võimalikult vähe toksilisi kemikaale.
- Looge vähem ohtlikud sünteesimeetodid – Võimalusel kasutage sünteesimise või biosünteesimise meetodeid, millel on väike või ei ole üldse toksilist mõju inimese tervisele ja keskkonnale.
- Kasutage turvalisemaid lahusteid ja reaktsioonide tingimusi – Leidke kõige värskem teave roheliste kemikaalide kohta, optimeerimaks oma protsessi ning tagamaks turvalisem töökeskkond.
- Õnnetuste vältimine – Valige ained, mis minimeerivad plahvatus- ja tulekahjuohtu ning vältige kemikaalide sattumist keskkonda.
Ökoloogilise jalajälje vähendamine
- Jäätmete vähendamine ja ärahoidmine – Töötage välja keemilise sünteesimise tehnikad, mis vähendavad või hoiavad ära jäätmete tekkimise. Parem on jäätmeid ära hoida, kui neid hiljem kõrvaldada.
- Stöhhiomeetrilsite reagentide asemel kasutage katalüsaatoreid – Katalüütilised reaktsioonid kasutavad loomupäraselt väiksemas koguses kemikaale kindla muundamise teostamiseks.
- Vähendage keemiliste derivaatide kasutamist – Kaitsegruppide või teiste ajutiste funktsionaalsuse modifikatsioonide kasutamine suurendab sünteesimisega kaasnevat jäätmete hulka.
- Sünteetiline efektiivsus (Aatomite kokkuhoid) – Tõhus keemiline protsess tagab maksimaalse koguse algmaterjali kasutamise lõpp-produktis, nii et mitte ükski aatom ei lähe raisku.
- Kasutage degradeeruvaid keemikaale – Vähendage mõjutusi keskkonnale kasutades kemikaale, mis on biolagunevad.
- Saastamise vältimise protsesside juhtimise kehtestamine – Ohtlike ainete tekkimise vältimiseks, võtke tarvitusele reaal-ajas analüüsimeetmed ja protsesside juhtimine sünteesimise käigus.
- Kasutage taastuvat tooret – Kasutage toormaterjali või taastuvat tooret (teiste protsesside jäätmeid või põllumajandusest pärit tooteid) iga kord kui see on tehniliselt või majanduslikult võimalik.
- Energiatõhususe edendamine – Energia kasutamise majandusliku- ja keskkonnamõju realiseerimine keemilistes protsessides ja alternatiivsete lahenduste arendamine mõju vähendamiseks.
Kui te soovite kaitsta oma tervist ja ka laboratooriumi keskkonda, siis soovitame teil oma huvides tutvuda Sigma-Aldrich tootevalikuga, muu hulgas:
- alternatiivenergia;
- biolagunevad polümeerid;
- boori ühendid ja modifikatsioonid;
- katalüsaatorid;
- voogkeemia;
- valik reagente ja solvente;
- ioonvedelikud;
- Novozyme;
- lahustite mahutite tagastamisprogramm.
2-Metüültetrahüdrofuraan (2-MeTHF)
Tõeliselt roheline alternatiiv diklorometaanile (DCM) ja tetrahüdrofuraanile (THF).
2-MeTHF saadakse taastuvatest allikatest, nagu maisitõlvikud ja suhkrurootolm. Organometallilise solvendina kasutamisel on 2-MeTHF nii ökonoomne kui ka keskkonnasõbralik alternatiiv tetrahüdrofuraanile.
Omadused & kasulikkus:
- Aprotoonne polaarne solvent
- Füüsikaliste omaduste poolest sarnaneb tolueeniga;
- Grignard reaktiivid lahustuvad paremini 2-MeTHF-s kui THF-s.
- Moodustab aseotroopidega rikastatud vee ning on seetõttu lihtsamini kuivatatav kui THF või DCM.
- Piiratud segunevus veega (4.1g/100g 23°C juures) võimaldab lihtsamat eraldamist ning veest kogumine vähendab jäätmete voogu.
- Kõrgem keemistemperatuur (80°C) võrreldes THF-ga. Kõrgem reaktsiooni temperatuur vähendab üldist reaktsiooni toimumise aega.
- Madal aurustumissoojus tähendab väiksemat solvendi kadu reaktsiooni destilleerimisel. Lisaks säästab see energiat destillatsiooni ja taastumise ajal.
Tertrahüdrofuraani alternatiiv organometallilistes reaktsioonides, nagu näiteks:
- Grignard
- Reformatsky
- Litiatsioon
- Hüdriidide vähendamine
- Metalli-katalüseeritud sidusreaktsioon (Heck, Stille, Suzuki)
Diklorometaani alternatiiv kaheastmelistes reaktsioonides, nagu näiteks:
- Alküülimine
- Amidatsioon
- Nukleofiilne asendusreaktsioon
Tsükopentüülmetüüleeter (CPME)
Keskkonnasõbralik alternatiiv tetrahüdrofuraanile, tert-butüülmetüüleetrile (MTBE), 1,4-dioksaanile ja teistele solventidele.
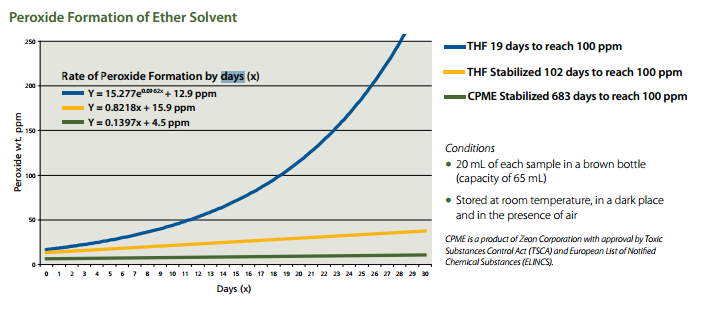
CPME on roheline lahendus kõigile, kes soovivad täiustada keemilisi protsesse, vähendada solventide jäätmevoogu ja parandada laboratooriumi ohutust, kuna CPME-l unikaalne koostis takistab peroksiidide teket.
Omadused & kasulikkus:
- Stabiilsem kui THF ja 2-MeTHF (nõuavad stabilisaatoreid):
- Takistab peroksiidide moodustimist;
- Vähendab peroksiidide testimise sagedust.
- Uudne hüdrofoobne eetrilahusti:
- Kasutatav paljudes organometallilistes reaktsioonides;
- Tagab parema tootlikkuse ja suurema selektiivsuse kui THF.
- Moodustab aseotroopidega rikastatud vee ning on seetõttu lihtsamini kuivatatav kui THF ja 2-MeTHF.
- Piiratud segunevus veega (1.1g/100g 23°C juures) võimaldab lihtsamat eraldamist ning veest kogumine vähendab jäätmete voogu.
- Kõrgem keemistemperatuur (106°C) võrreldes THF ja 2-MeTHF-ga. Kõrgem reaktsiooni temperatuur vähendab üldist reaktsiooni toimumise aega.
- Madal aurustumissoojus tähendab väiksemat solvendi kadu reaktsiooni destilleerimisel. Lisaks säästab see energiat destillatsiooni ja taastumise ajal.
CPME rakendused:
- Assümeetriline Michael‘i alküülimine
- R2CuLi Michael‘i lisand
- Kiraalamiidi alküülimine
- Glükosideerimine
- NaBH4 assümeetriline hüdrogeenimine
- Hüdrosilüülimine RU cat teel
- Nukleofiilsed reaktsioonid
- Amiidisüntees kloriidhappe ja amiini regeerimise kaudu
- Sillülatsioon ja desillülatsioon
- Süsinikanioonide raeaktsioonid aldehüüdidega
- Debensülatsioon
- Amiini alküülimine
- Fenoolide selektiivne metüülimine
- Alkoholi broomimine PBr3-ga
- Sulfonüülkloriidi süntees sulfoonhappe reageerimisel PCl5-ga
- Reaktsioonid metallidega
- Ketooni reaktsioon kasutades NaBH4
- Atsetüleeni reaktsioon Ti(OR)4-ga
- Reakstioonid n-BuLi või liitiumdiisopropüülamiidiga
- Trikloroatsetaadi radikaalne tsüklistamine CU cat-ga
- Etüülbensoate vähendamine liitiumalumiiniumhüdriidiga
- Naatriumdispersiooni moodustamine
- Molekulisisene Alder-ene reaktsioon ZnCl2-ga